光热驱动数字PCR技术绘制外泌体致癌microRNA表达谱,构建前列腺癌早筛平台
2022-10-13 17:41:48
面向肿瘤早筛的快速发展,叶方富团队在近期在《Advanced Functional Materials》(IF = 19.924)期刊上发表论文“Screening Prostate Cancer Cell-Derived Exosomal MicroRNA Expression with Photothermal-Driven Digital PCR”,论文链接为:https://onlinelibrary.wiley.com/doi/abs/10.1002/adfm.202207879。
 前列腺癌(PC)是男性第二大恶性肿瘤,每年造成30多万人死亡。目前的诊断和监测方法由于不适、低特异性和准确性而受到限制。外泌体介导肿瘤转移、炎症反应、信号转导、抗原表达等各种细胞间生理活动。它因外膜保护而稳定,且在体液中浓度高,这使它成为肿瘤诊断、预后和治疗的一个良好生物标记物来源。本论文首先提出一种基于纳米粒子的亲和素-生物素结合的非特异性外泌体捕获方法,从而便捷地获得完整的外泌体RNA文库。为了灵敏、简单地检测目标,我们通过嵌入具备优良光热效应的MXene和磁性纳米粒子复合材料开发出不同响应程度的温敏微载体,用于构建近红外光驱动的数字PCR检测技术。搭建基于Arduino芯片的程序可控的近红外光输出器件,实现自动化、按需的辐射以推动微载体完成PCR热循环过程;并定制快速PCR程序,升温速率快于传统PCR仪。双荧光探针协同的光热驱动的多重数字PCR技术定量描绘出外泌体中致癌基因microRNA-21-5p、microRNA-574-3p和PC转移通路的microRNA-375-3p相对于看家基因microRNA-30a-5p的指纹谱图。结果表明,PC样本中的三个靶点水平分别比健康细胞系来源的结果上调7-210倍。相比而言,新方法的检测下限比荧光PCR法改善超过二十倍,并且能从低丰度中稳健地识别五倍以内的微小表达差异。因此,这种快速、灵敏、通用的外泌体microRNA基因分型方法具有潜在的临床应用价值。
前列腺癌(PC)是男性第二大恶性肿瘤,每年造成30多万人死亡。目前的诊断和监测方法由于不适、低特异性和准确性而受到限制。外泌体介导肿瘤转移、炎症反应、信号转导、抗原表达等各种细胞间生理活动。它因外膜保护而稳定,且在体液中浓度高,这使它成为肿瘤诊断、预后和治疗的一个良好生物标记物来源。本论文首先提出一种基于纳米粒子的亲和素-生物素结合的非特异性外泌体捕获方法,从而便捷地获得完整的外泌体RNA文库。为了灵敏、简单地检测目标,我们通过嵌入具备优良光热效应的MXene和磁性纳米粒子复合材料开发出不同响应程度的温敏微载体,用于构建近红外光驱动的数字PCR检测技术。搭建基于Arduino芯片的程序可控的近红外光输出器件,实现自动化、按需的辐射以推动微载体完成PCR热循环过程;并定制快速PCR程序,升温速率快于传统PCR仪。双荧光探针协同的光热驱动的多重数字PCR技术定量描绘出外泌体中致癌基因microRNA-21-5p、microRNA-574-3p和PC转移通路的microRNA-375-3p相对于看家基因microRNA-30a-5p的指纹谱图。结果表明,PC样本中的三个靶点水平分别比健康细胞系来源的结果上调7-210倍。相比而言,新方法的检测下限比荧光PCR法改善超过二十倍,并且能从低丰度中稳健地识别五倍以内的微小表达差异。因此,这种快速、灵敏、通用的外泌体microRNA基因分型方法具有潜在的临床应用价值。
该论文为我院与温州医科大学附属第一医院联合医学转化中心、中国科学院物理研究所、中国科学院大学的合作工作。第一作者为我院的副研究员张乐翔,通讯作者为中科院物理所王晓晨、樊琪慧副研究员和我院的叶方富研究员。该论文获得中国科学院青年创新促进会(No. 2021007)、 浙江省自然科学基金(LGF22C100003)、国科温州研究院启动项目(WIUCASQD2021012)的支持。
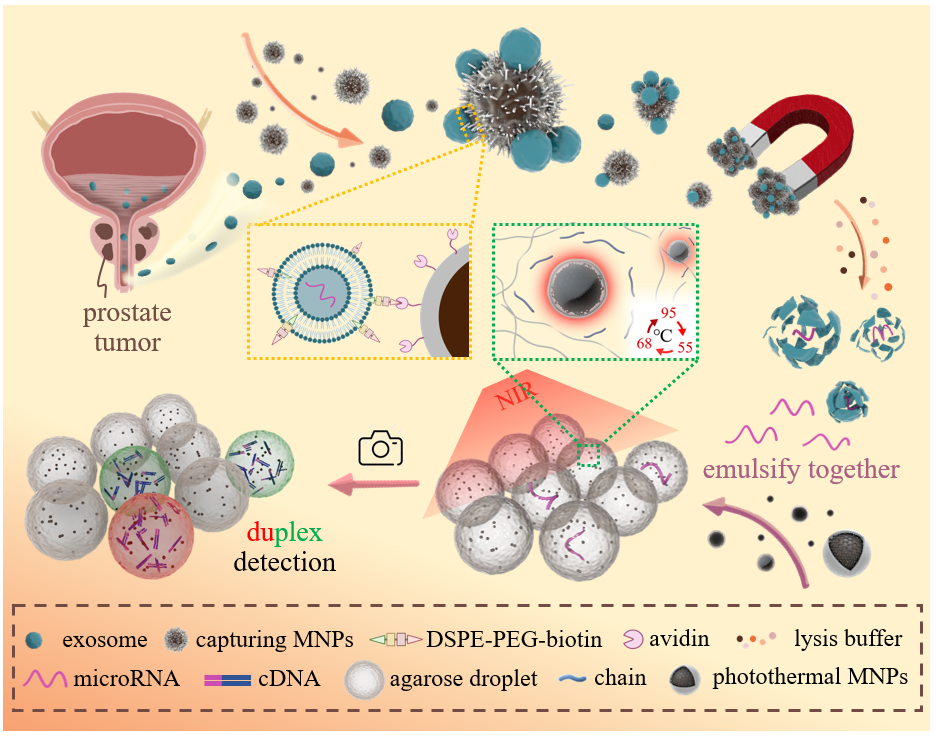
图 光热驱动多重数字PCR技术绘制外泌体microRNA谱图

该论文为我院与温州医科大学附属第一医院联合医学转化中心、中国科学院物理研究所、中国科学院大学的合作工作。第一作者为我院的副研究员张乐翔,通讯作者为中科院物理所王晓晨、樊琪慧副研究员和我院的叶方富研究员。该论文获得中国科学院青年创新促进会(No. 2021007)、 浙江省自然科学基金(LGF22C100003)、国科温州研究院启动项目(WIUCASQD2021012)的支持。

图 光热驱动多重数字PCR技术绘制外泌体microRNA谱图



