用于肿瘤药物递送的高核发光镧系纳米笼
目前,全球六分之一的死亡是由癌症造成的,已有诸多研究者们致力于探索药物输送系统,通过改善药物靶向性、控制药物释放和减少脱靶效应来减轻这种公共卫生负担。基于纳米材料的药物载体在这方面受到了极大的关注,它们能够通过增强的渗透性和保留(EPR)效应选择性地将治疗药物输送到实体肿瘤中。迄今为止,纳米乳剂、纳米颗粒和纳米胶束已被用作药物载体。这些药物大多粒径相对较大,通常直径≥100 nm。然而,一些肿瘤,如乳腺癌和胰腺癌,具有非常小的血管孔径(50 - 60 nm),这就限制了较大的纳米材料(即直径>50 nm)有效地进入肿瘤组织。更复杂的问题是,大多数大型纳米材料通常无法穿透构成肿瘤间质的致密细胞外基质。因此,需要相对较小的载体,以增强治疗药物进入肿瘤组织的递送。更重要的是寻求一种能够对肿瘤进行准确定位和可视化的药物载体。
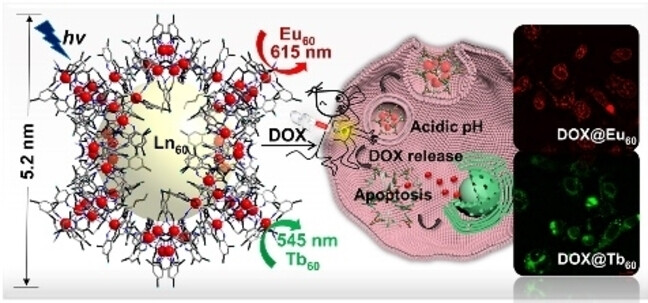
我院李花琼研究员团队与温州大学杨小平教授、杨植教授、美国德克萨斯大学奥斯汀分校Jonathan L. Sessler教授等团队开展合作研究,制备了超小发光亚胺基镧系元素纳米笼Eu60和Tb60(统称为Ln60),旨在封装抗癌化疗药物用于肿瘤治疗。制备的纳米笼具有适合阿霉素(DOX)包封的大空腔,DOX@Ln60纳米笼直径约5.2 nm,由具有柔性- C2H4NHC2H4 -骨架的链状希夫碱配体构成。这些Ln60配合物构成了由席夫碱配体构成的创纪录的高核镧系元素团簇。它们具有中空的纳米笼结构,具有大的内部空隙(~1.5 nm),能够容易地加载DOX。此外,它们可以在小鼠TNBC模型中有效地给药和成像。据我们所知,这是第一个将高核镧系纳米团簇应用于肿瘤检测治疗的报道。

DOX@Ln60被可以乳腺癌细胞有效地摄取,使细胞可见通过Ln(III)的本征发光特性。一旦摄取,酸性细胞内微环境促进亚胺键断裂和负载的DOX的释放。DOX@Ln60能够抑制DNA复制,触发肿瘤细胞的凋亡。在小鼠三阴性乳腺癌(TNBC)模型中,DOX@Ln60被发现能抑制肿瘤生长对正常组织的副作用微不足道。因此,目前的纳米笼为肿瘤成像和治疗的精确纳米药物的发展指明了道路。
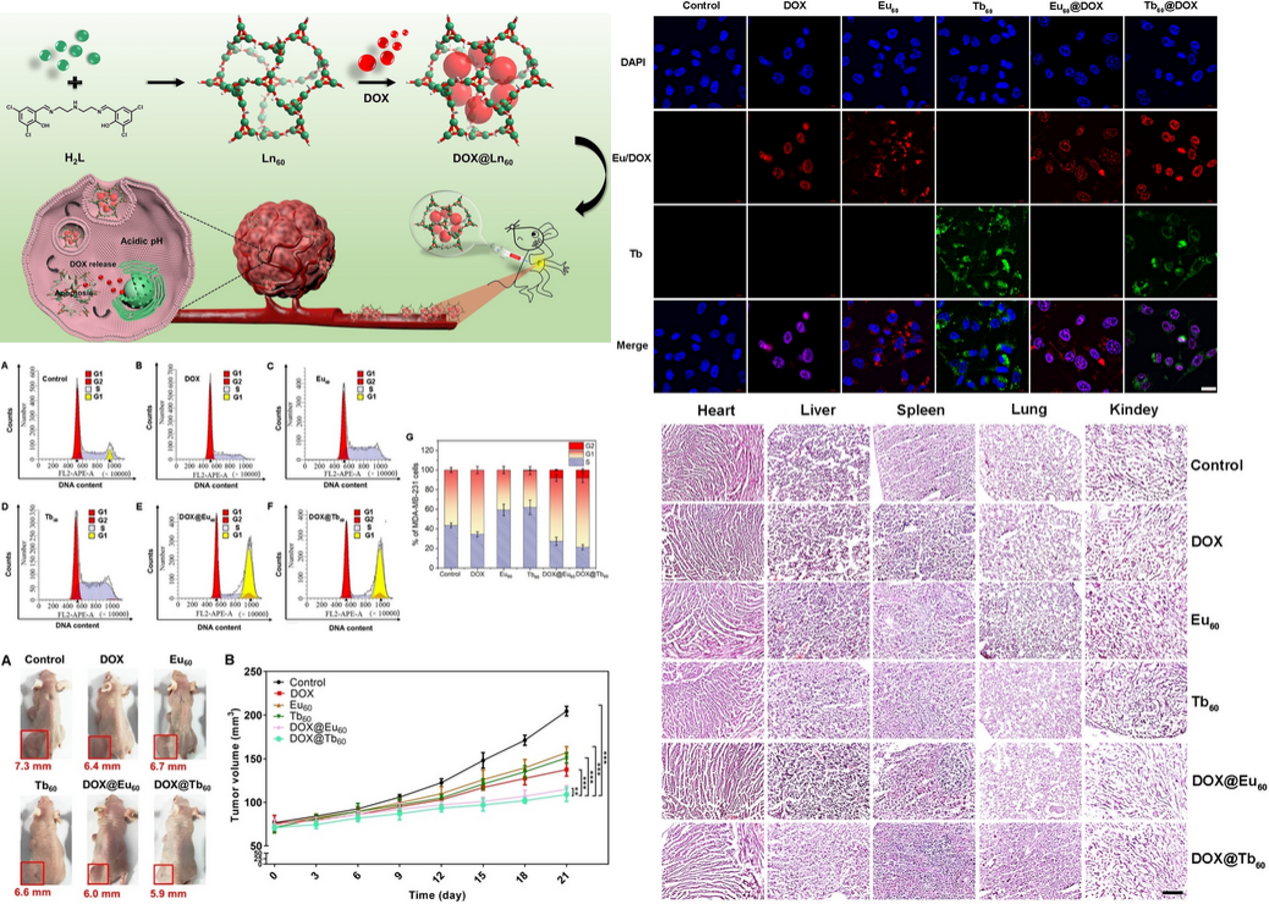
综上所述,通过镧系发光发现该结构物(DOX@Ln60)可以有效地进入乳腺癌细胞,并且很容易被观察到,在体内外均观察到明显的肿瘤抑制作用,在正常组织中未见明显不良反应。鉴于其精确的化学成分和杀死肿瘤细胞方面显示的功效,DOX@Ln60纳米笼可能为当前的肿瘤治疗和药物递送策略提供有用的策略。
相关科研成果近期以High-nuclearity luminescent lanthanide nanocages for tumor drug delivery为题发表在Angewandte Chemie International Edition (IF:16.6)。该工作得到国家自然科学基金、浙江省自然科学基金和国科温州研究院启动项目等项目资助。



